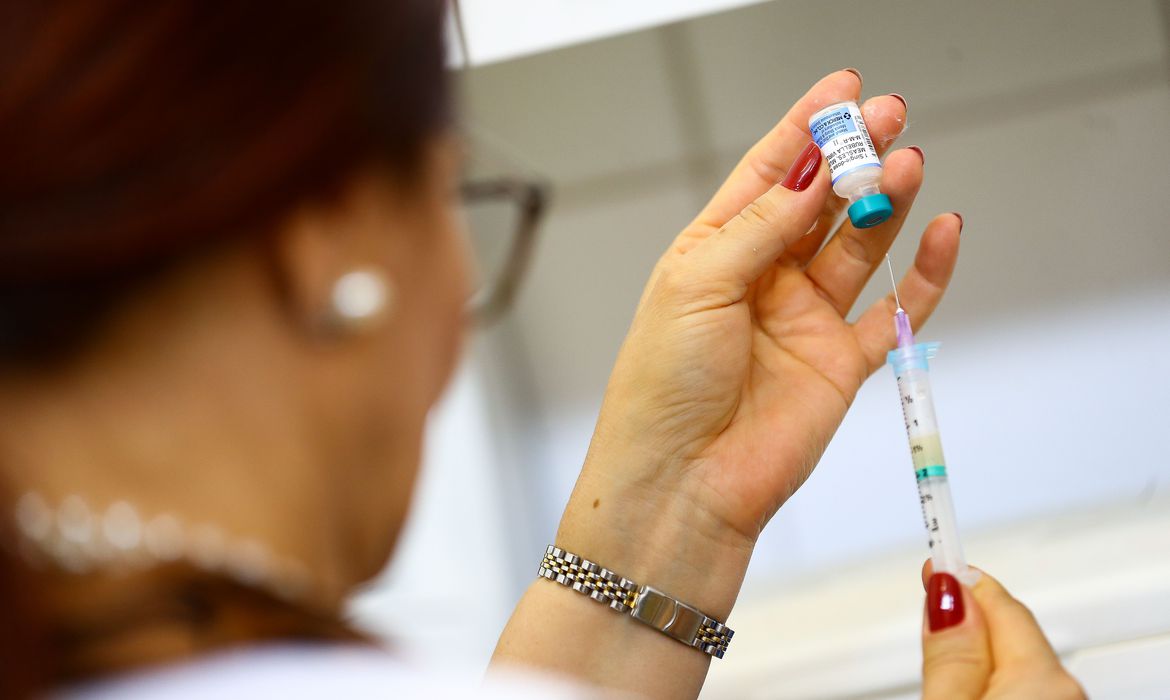
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu os dados referentes aos estudos não-clínicos e clínicos das fases I e II da vacina contra a Covid-19 desenvolvida pelas empresas Pfizer/BioNTech. A documentação foi incluída no processo de submissão contínua iniciado nesta semana.
A Anvisa tem até 20 dias para analisar os documentos, contados a partir da data do protocolo. Segundo a agência reguladora, a submissão contínua ainda não é o pedido de registro da imunização. Pelo procedimento, os dados técnicos deverão ser encaminhados à Anvisa conforme forem gerados.
Dessa maneira, as empresas interessadas no registro de vacinas contra Covid-19 não precisão ter em mãos todos os documentos reunidos para apresentá-los à autarquia
Fonte: Brasil 61
 EXPORTAÇÃO União Europeia deixa Brasil fora de exportação de carnes por exigências sanitárias
EXPORTAÇÃO União Europeia deixa Brasil fora de exportação de carnes por exigências sanitárias  SEGURANÇA PÚBLICA Lula anuncia programa de R$ 11 bilhões para reforçar combate ao crime organizado
SEGURANÇA PÚBLICA Lula anuncia programa de R$ 11 bilhões para reforçar combate ao crime organizado  ANISTIA Contra decisão do STF, líder do PL articula PEC para anistiar condenados do 8 de Janeiro
ANISTIA Contra decisão do STF, líder do PL articula PEC para anistiar condenados do 8 de Janeiro Mín. 22° Máx. 33°



