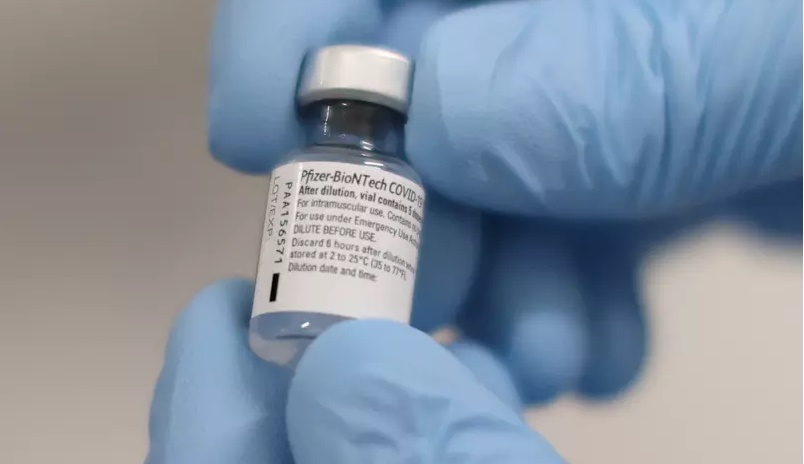
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu neste sábado (6) o pedido de registro definitivo da Comirnaty, vacina contra a Covid-19 desenvolvida pela farmacêutica norte-americana Pfizer em parceria com a empresa alemã de biotecnologia BioNtech.
"O registro concedido pela Anvisa é o sinal verde para que a vacina seja comercializada, distribuída e utilizada pela população, nos termos da indicação estabelecida na bula", disse a Anvisa em seu site.
"Ou seja, o registro é a avaliação completa com dados mais robustos dos estudos de qualidade, eficácia e segurança, bem como do plano de mitigação dos riscos e da adoção das medidas de monitoramento", completou a Anvisa.
Com a oficialização do pedido de registro definitivo pela farmacêutica, a Anvisa tem 60 dias para avaliar a documentação. No entanto, a expectativa é que esse prazo seja reduzido, considerando as informações que a agência já recebeu por meio do procedimento de submissão e análise contínua.
De acordo dados do painel de monitoramento da agência, até 8h deste sábado (6) já foi concluída a análise de 34,38% dos documentos enviados pela farmacêutica, estão pendendes de complementação outros 50,21%, não tem dados suficientes 5,21% e não foram apresentados 10,21%.
Em nota, a Pfizer confirmou que deu início ao processo de registro definitivo da vacina BNT162b2 contra a COVID-19, desenvolvida pela empresa e pela BioNTech, junto à Anvisa.
“O pedido de registro da vacina junto à Anvisa é a etapa final do processo de submissão contínua estabelecido pela Agência para acelerar os registros de vacinas contra a Covid-19. A companhia continuará trabalhando junto com a Anvisa para que esse processo transcorra da melhor maneira possível, sempre pautados por critérios técnicos e científicos”, afirmou, na nota, Márjori Dulcine, diretora médica da Pfizer Brasil.

A empresa esclareceu que a submissão tem como base dados de segurança e eficácia avaliados de aproximadamente 44 mil participantes do estudo, que foram acompanhados por dois meses, em média, após a segunda dose da vacina experimental.
“O estudo clínico de fase 3 com a BNT162b2, que conta com a tecnologia de mRNA desenvolvida pela BioNTech, foi realizado em 150 centros nos EUA, Alemanha, Turquia, África do Sul, Brasil e Argentina”, destacou a empresa.
No Brasil, participaram 2,9 mil voluntários e os trabalhos foram conduzidos pelo Centro Paulista de Investigação Clínica (Cepic), em São Paulo, e pelas Obras Assistenciais Irmã Dulce, em Salvador.
A vacina da Pfizer/BioNtech mostrou 95% de eficácia e não apresentou problemas de segurança, segundo análise final da terceira e última fase de testes clínicos da vacina divulgada em novembro.
 COMBUSTÍVEIS Governo Lula anuncia subsídio de até R$ 0,89 no litro da gasolina
COMBUSTÍVEIS Governo Lula anuncia subsídio de até R$ 0,89 no litro da gasolina  HOMENAGEM Patoense Antônio Coelho é homenageado na Assembleia Legislativa de São Paulo durante solenidade pelo Dia Nacional do Agente de Trânsito
HOMENAGEM Patoense Antônio Coelho é homenageado na Assembleia Legislativa de São Paulo durante solenidade pelo Dia Nacional do Agente de Trânsito  EXPORTAÇÃO União Europeia deixa Brasil fora de exportação de carnes por exigências sanitárias
EXPORTAÇÃO União Europeia deixa Brasil fora de exportação de carnes por exigências sanitárias Mín. 21° Máx. 32°